La ventilation spontanée normale
En ventilation spontanée, lorsque nous inspirons, nous créons une petite dépression dans notre thorax qui attire l’air de l’extérieur vers nos poumons. L’expiration est neurologiquement l’inhibition de l’inspiration. L’effort inspiratoire s’arrête et le thorax et ses poumons se rétractent “passivement” via les forces élastiques du système. À la fin de l’expiration, la pression dans les voies aériennes est nulle. À cet instant très précis, la pression dans les voies aériennes est égale à la pression atmosphérique, il n’y a pas de flux d’air entre l’extérieur et les poumons. À ce moment, le volume dans les poumons est appelé la capacité résiduelle fonctionnelle (CRF)
La PEP
La PEP est une pression positive (résiduelle) à la fin de l’expiration dans les voies aériennes du patient.
Dans la majorité des cas, on emploie le terme PEP en signifiant une pression appliquée par une machine sur les voies aériennes du patient. Le patient peut-être réveillé et en ventilation spontanée avec un masque appliqué sur ses voies aériennes ou carrément sédaté, curarisé, placé sous ventilation mécanique via une intubation trachéale.
Lorsqu’une PEP est appliquée au patient, sa CRF est augmentée car des alvéoles restent remplies du fait de l’existence d’une pression s’opposant à leur vidange. Ce volume résiduel est utile pour conserver les alvéoles au-dessus de ce qu’on appelle le volume de fermeture. Le volume de fermeture est le volume critique en deça duquel, l’alvéole se collabe. Lorsque de nombreuses alvéoles se collabent, il y a formation d’atélectasies. Il existe alors des zones de poumons qui ne sont plus ventilées alors qu’elles restent perfusées, créant ainsi du shunt.
La PEP vise à éviter le collapsus alvéolaire et ne sert pas “à réouvrir” des alvéoles collabées.
La PEP réglée sur les machines est aussi appelée PEPe pour PEP extrinsèque, c’est-à-dire venant de l’extérieur du patient.
Dans certaines pathologies comme la BPCO, il peut exister une PEPi pour PEP intrinsèque. La PEPi est parfois appelée auto-PEP. Chez le sujet sain, il n’y a pas de PEPi. L’hyperinflation dynamique est une grande cause de génération d’une PEPi en pathologie.
La PEP totale est la pression positive (résiduelle) à la fin de l’expiration dans les voies aériennes du patient. Elle correspond à l’ensemble des effets de la PEPi et de la PEPe.
La BPCO
Je vous copie-colle la définition de Wikipédia : la BPCO est caractérisée par une obstruction lente et progressive des voies aériennes et des poumons, associée à une distension permanente des alvéoles pulmonaires avec destruction des parois alvéolaires. La BPCO est caractérisée par la diminution non complètement réversible des débits expiratoires.
L’hyperinflation dynamique
En cas de BPCO (a fortiori si exacerbation), l’inflammation chronique réduit le diamètre des bronches. L’air rentre de façon actif grâce à la force musculaire en ventilation spontanée, ou du fait d’une pression positive en ventilation artificielle, mais les alvéoles ne se vident pas bien, car l’expiration passive ne suffit pas à pousser tout le gaz alvéolaire dehors. Il existe une diminution du débit expiratoire.
Il y a trois grands facteurs qui jouent sur l’hyperinflation dynamique : le volume courant (Vt), l’augmentation du produit (résistance * compliance) appelé constante de temps ϑ et le temps expiratoire (Te).
- Le Vt : plus il y a d’air qui rentre dans le poumon, plus y a un risque qu’il n’arrive pas à sortir à cause de la diminution du débit expiratoire
- ϑ = résistance * compliance. Lorsque les résistances sont élevées, c’est plus compliqué pour l’air de franchir l’obstacle dans le sens intérieur -> extérieur. Et une compliance élevée traduit un poumon qui se laisse distendre facilement, mais qui n’aura pas beaucoup de force pour se rétracter. L’élastance, la capacité de se rétracter, est l’inverse de la compliance.
- Le Te : si le temps expiratoire est court, les alvéoles n’ont pas le temps de se vider.
L’hyperinflation dynamique, c’est le fait que de l’air reste piégé dans les alvéoles au fil des cycles respiratoires. Cet air dans les alvéoles génère une pression positive en fin d’expiration : c’est la PEP intrinsèque.
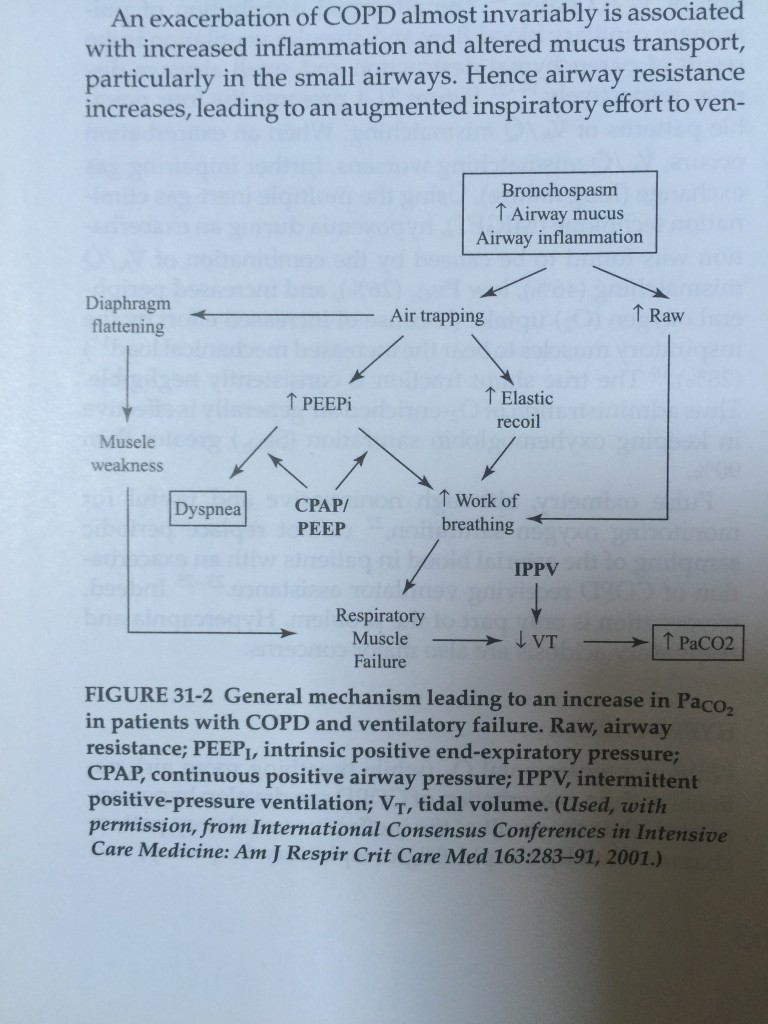
Les conséquences de l’hyperinflation dynamique
Lorsqu’il y a de l’hyperinflation dynamique, le volume résiduel augmente et les muscles respiratoires sont anormalement étirés. Dans cette configuration, leur fonctionnement est moins bon.
Par ailleurs, le thorax est lui aussi sous tension, ses forces de rétractions élastiques sont plus fortes et l’inspiration devra vaincre cette force supplémentaire.
Enfin, l’inspiration démarrera sur une portion moins favorable de la courbe pression-volume. En effet, lorsqu’il existe un volume résiduel, la compliance du poumon est moins bonne (il faut une plus grande différence de pression pour générer une variation de volume) et donc là encore, il faut faire un effort inspiratoire plus grand.
Au total, les muscles sont dans une mauvaise posture pour travailler et ils doivent fournir un plus grand effort pour faire rentrer l’air dans les poumons. C’est ce qu’on appelle l’augmentation du travail respiratoire.
Retenez (de façon caricatural) que si les passagers d’une rame de métro ne peuvent pas descendre parce que les portes ne s’ouvrent pas normalement, il va d’autant plus être compliqué de faire rentrer des nouveaux passagers pourtant très motivés !
La PEPi peut également avoir des conséquences hémodynamiques. L’augmentation de la pression intrathoracique peut gêner le retour veineux et diminuer le débit cardiaque.
Il existe également des difficultés en ventilation artificielle à type d’asynchronies et de difficultés pour déclencher des cycles respiratoires.
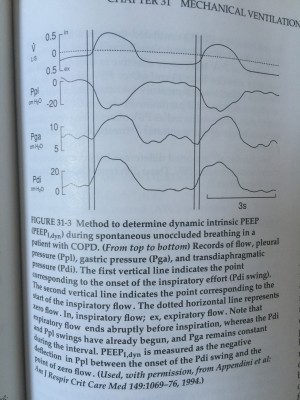
Rechercher la PEPi
Chez un patient en ventilation spontanée, c’est difficile.
Dès lors que le patient a un support ventilatoire, il faut observer la courbe de débit expiratoire. Si le débit ne rejoint pas la ligne de base ; autrement dit si l’expiration est coupée par une nouvelle inspiration, il faut suspecter la création d’une PEPi.
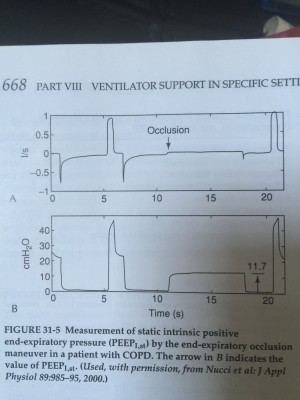
Chez un patient profondément sédaté, la réalisation d’un plateau expiratoire peut déceler la PEPi.
Prise en charge classique de ces patients avec une limitation du débit expiratoire
Administration de bronchodilatateur (béta-mimétique). Les modalités d’aérosolisation sont très importantes et sortent du cadre de ce billet. Néanmoins, je pense que le spray de ventoline dans la sonde d’intubation est une vaste blague (la molécule ne peut pas progresser comme ça jusqu’aux bronches).
Je viens d’une école où les atropiniques sont regardés de travers donc je n’en prescris pas.
Corticothérapie intraveineuse.
En ventilation mécanique type VAC : fréquence basse, ratio I/E =< ⅓, Vt à 6 ml/kg avec une hypercapnie permissive. Réglages des alarmes ad hoc (Pcrête forcément élevée et toujours faire attention au plateau =< 30cmH2O)
Traitement d’un facteur déclenchant (infection par exemple)
N.B. j’ai observé dans ma pratique beaucoup de complications digestives à type de syndrome subocclusif. Je pense que c’est quelque chose qu’il faut surveiller et anticiper (nutrition, laxatifs, diminution des morphiniques, etc.)
Anecdote sur un sujet connexe.
J’ai eu à prendre en charge un patient polypathologique avec une sténose trachéale en détresse respiratoire. Il s’est révélé difficile à ventiler et à intuber. Juste après l’intubation, bradycardie extrême et catastrophe hémodynamique.
J’ai immédiatement débranché le ventilateur de la sonde d’intubation et j’ai appuyé plusieurs fois sur le thorax du patient vigoureusement.
L’hémodynamique s’est immédiatement améliorée.
Nous avions fait rentrer plein d’air dans son thorax qu’il n’avait pas pu expirer. Je pense qu’il y avait une sorte de tamponnade gazeuse. (Je lutte tous les jours contre les excès de la ventilation au masque trop vigoureuse/rapide…)
L’analogie de la cascade (waterfall model)
L’analogie de la cascade est un modèle monocompartimental proposé par un grand pneumologue américain nommé Tobin. Le débit expiratoire est assimilé au débit d’une cascade. Le débit dépend de la pression du lac d’amont et pas de celui du lac d’aval. Le niveau du lac d’aval peut monter, le débit de la cascade ne changera pas tant que le lac d’aval ne sera pas au niveau du lac d’amont. C’est « tout ou rien ».
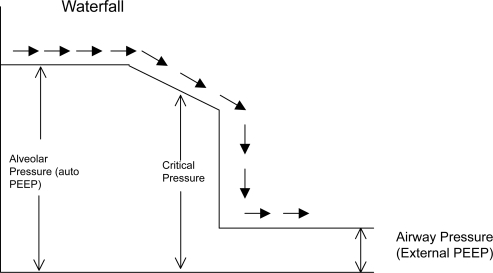
Ainsi, selon cette analogie, la PEPe n’a pas d’influence sur la ventilation du patient tant qu’elle n’atteint pas le niveau de la PEPi.
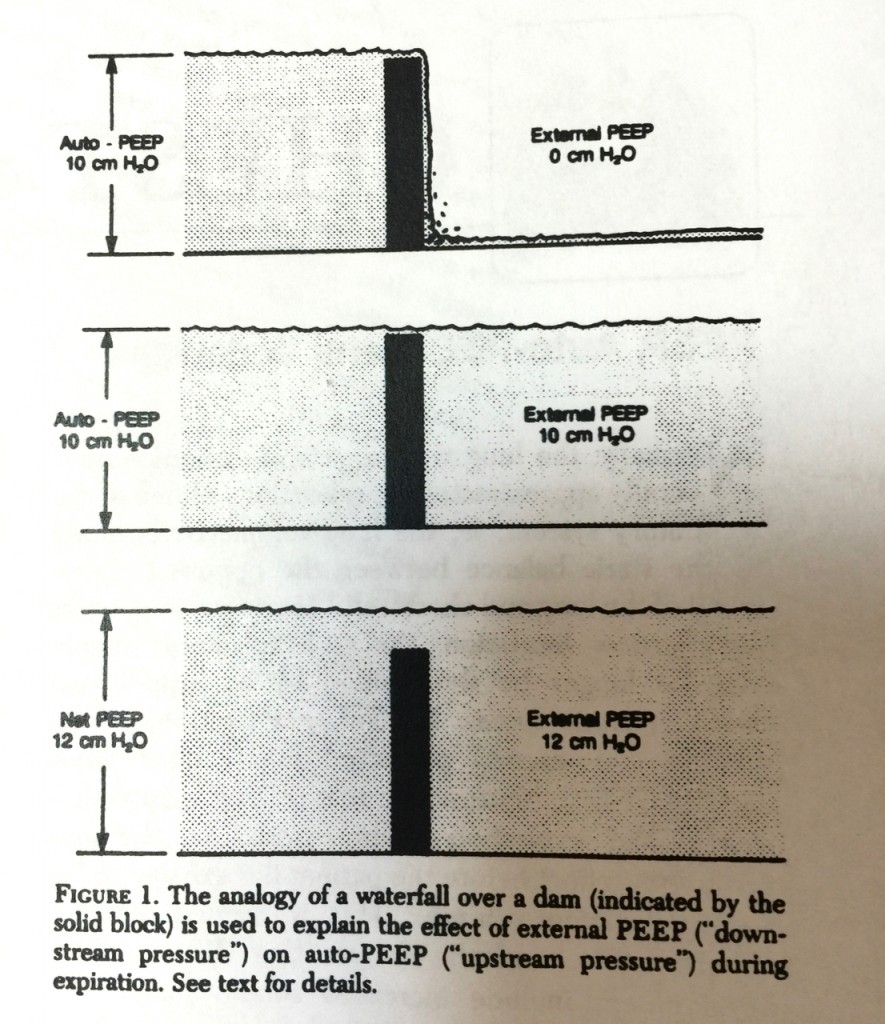
Effets de la PEPe chez un patient avec une limitation du débit expiratoire
Lorsque le patient est en ventilation spontanée et qu’il a une PEPi, le premier intérêt de régler une PEPe est de faciliter la prise de cycles respiratoires spontanés. En effet, la PEPi est une pression qu’il faut vaincre avant d’atteindre le seuil de déclenchement (trigger) d’un cycle respiratoire programmé sur la machine (en VS-AI ou en VAC). La PEPe vient compenser cette difficulté en décalant le seuil de déclenchement vers le haut. Si un patient à une PEPi = 8 cmH20, il va devoir combattre ces 8 cmH20 avant d’atteindre une pression nulle, puis produire une pression négative pour déclencher un cycle. En mettant une PEPe à 8 cmH20 qui égale la PEPi, le patient a moins d’effort à faire puisque la PEPe est égale à sa PEPi, il réussira mieux à déclencher un cycle.
Ensuite, on a prêté à la PEPe d’autres vertus pour améliorer la ventilation de ces patients, mais là c’est plus nébuleux, et les études sur le sujet comportent peu de patients.
J’ai trouvé un travail publié dans Crit Care Med en 2005 qui a testé l’effet de la PEPe chez des patients présentant une diminution du débit expiratoire. Les patients étaient curarisés.
La PEPe a été augmentée de zéro jusqu’à 1,5*PEPi avec une surveillance de plusieurs paramètres (gaz du sang, hémodynamique, mécanique ventilatoire.)
La principale conclusion de ce travail avec un faible effectif (8 patients !) c’est que l’effet de la PEPe n’est pas univoque. Les auteurs ont classé les résultats en trois catégories :
- La réponse biphasique : tant que la PEPe n’excédait pas la PEPi, les paramètres étaient stables. Lorsque la PEPe dépassait la PEPi, ils observaient une aggravation de l’inflation thoracique.
Aggravation
- d’emblée de l’hyperinflation thoracique : quelque soit le niveau de PEPe, la situation empirait
- La réponse paradoxale : la PEPe a amélioré l’inflation thoracique avec une baisse de la pression de plateau.
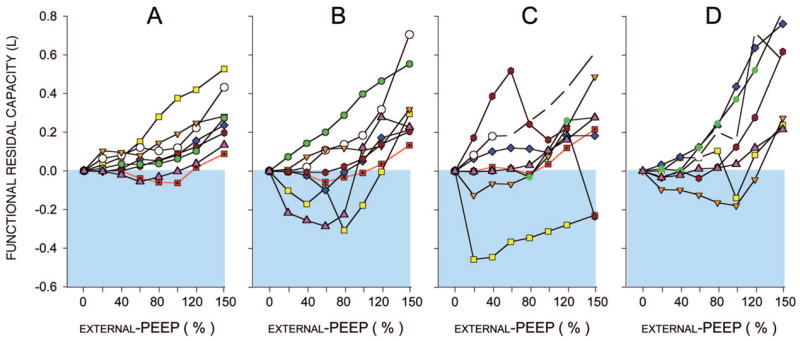
Changes in functional residual capacity (FRC) assessed by inductive plethysmography. Individual responses along the incremental external positive end-expiratory pressure (PEEP) steps, from zero external-PEEP (reference) to a value matching 150% of intrinsic-PEEP measured at zero external-PEEP conditions. A, tidal volume (VT) = 6 mL/kg, respiratory rate (RR) = 6 breaths/min; B, VT = 6 mL/kg, RR = 9 breaths/min;C, VT = 9 mL/kg, RR = 6 breaths/min; D, VT = 9 mL/kg, RR = 9 breaths/min. The FRC measured at zero external-PEEP was considered as the reference. Points inside the gray zone indicate the occurrence of a paradoxic response.
Ainsi, il est possible que l’application d’une PEPe améliore la ventilation d’un patient avec une importante PEPi mais ce choix thérapeutique ne peut pas être recommandé systématiquement, et il ne peut s’agir que d’un test avec une incrémentation progressive de la PEPe et surveillance de l’évolution hémodynamique et ventilatoire.
Ce travail va un peu à l’encontre de la célèbre analogie de la cascade. Les explications des auteurs sont les suivantes :
- l’analogie de la cascade est un modèle unicompartimental qui ne reflète pas l’hétérogénéité pulmonaire
- la PEPe pourrait limiter le collapsus des bronchioles dans certaines zones
- un secteur pulmonaire sans limitation du débit expiratoire pourrait influencer positivement une zone qui a une limitation du débit expiratoire. En étant caricatural, une alvéole bien ouverte (grâce à la PEPe) attachée à un système bronchique avec peu de résistance pourrait aider la vidange d’alvéoles adjacentes qui subissent une limitation du débit expiratoire. Les alvéoles d’un système moins malade appuieraient en quelque sorte sur les alvéoles aux bronches les plus malades.
- la PEPe permettrait d’augmenter la rigidité bronchique et de faciliter le débit expiratoire
- la PEPe permettrait de ralentir quelque peu le flux expiratoire. En ralentissant le flux gazeux engendre moins de variation de pression dans la bronche rétrécie ce qui diminuerait son risque de collapsus (cf Bernouilli)
En conclusion :
- La PEPi a d’autant plus de risque d’être là que la patient est instable ou avancé dans sa pathologie
- Chez un patient BPCO qui peut déclencher son respirateur, la PEPe a un grand intérêt pour contrecarrer la PEPi.
- Chez un patient BPCO, la PEPe peut améliorer la PEPi mais ça n’est pas prévisible et elle peut aussi aggraver les choses.
- Si la PEPe a un effet, c’est probablement via le système bronchique.
- Au bloc opératoire avec un patient BPCO/asthmatique stable, la PEPe est à discuter au cas par cas. Avec un niveau de preuve moi-même comme on dit sur Twitter, j’aurais tendance à ne pas trop me focaliser sur ce point, il y a d’autres défis !
- En réanimation, avec un patient très grave, la question prend tout son sens.
Le coin du bistrot :
- en Médecine, on croit parfois faire un truc formidable avec de la poudre de perlimpimpin, le petit truc miracle. La PEPe n’est pas un truc miracle chez le BPCO. Il faut avant tout se focaliser sur le traitement de fond du bronchospasme.
- lorsque vous ventilez, notamment au masque, un patient qui fait un bronchospasme, même si la situation est stressante, retenez-vous de le ventiler à 40 de fréquence ! Oxygénez le patient, appelez à l’aide et faite ce qu’il faut, mais de grâce ayant dans un coin de votre tête l’idée qu’il n’expire pas tout l’air que vous lui insufflez.
Une réponse sur « Faut-il mettre une PEP au patient BPCO ? »
Tres bien, vision critique et scientifique dans un esprit anecdotique qui remet en question la PEPe conçu par certains comme evidence